Местное применение мочевины в уходе за кожей: обзор
Леонардо Челлено, Католический университет Святого Сердца, Рим, Италия, WILEY Дерматологическая терапия, 19 июля 2018 г., DOI: 10.1111/dth.12690
Аннотация
Нарушения барьерной функции связывают с рядом кожных заболеваний, включая ксероз, атопический дерматит и псориаз. Мочевина, компонент естественного увлажняющего фактора кожи, играет важную роль в сохранении гидратации и целостности кожи. Несколько исследований изучали влияние мочевины в клинических условиях. В настоящей статье мы обобщаем доступные клинические данные о влиянии мочевины на поддержание здоровья кожи и лечение кожных заболеваний. В более низких дозах (≤10%) препараты местного применения, содержащие мочевину, действуют как увлажнитель кожи, в то время как при более высоких концентрациях (>10% мочевины) препараты на основе мочевины оказывают кератолитическое действие. (например, Аквапилинг (aquapiling.net)) Мочевина также полезна при комбинированной терапии противовоспалительными и противогрибковыми препаратами в силу своей активности в качестве усилителя проникновения.
КЛЮЧЕВЫЕ СЛОВА
атопический дерматит, вульгарный ихтиоз, кератолитическое средство, увлажняющее средство, онихомикоз, псориаз, мочевина местного применения, ксероз
ВВЕДЕНИЕ
Роль кожи заключается в защите тела от вредного воздействия окружающей среды при сохранении соответствующих механических свойств, в том числе эластичности. Здоровая кожа характеризуется эффективным контролем потери воды, что позволяет поддерживать хороший уровень увлажнения и, следовательно, прочный физический и химический барьер (Verdier-Sévrain & Bonté, 2007).
Мочевина – это полярная гигроскопическая молекула, эндогенно вырабатываемая человеческим организмом и естественным образом обнаруживаемая в коже. Мочевина образуется в результате метаболизма белков и других органических соединений азота и выделяется с мочой и потом (Kapuscinska & Nowak, 2014; Mosher, 1933). Как один из компонентов натурального увлажняющего фактора (NMF), мочевина способствует сохранению здорового уровня увлажнения кожи. Несмотря на постоянное открытие новых ингредиентов и новых составов для ухода за кожей, мочевина по-прежнему остается одной из самых полезных молекул, доступных дерматологам из-за ее молекулярных и функциональных характеристик. В настоящей статье мы представляем обзор клинических данных, подтверждающих использование мочевины для поддержания целостности кожи и лечения заболеваний, связанных с дисфункцией кожного барьера.
МОЧЕВИНА И КОЖА
Роговой слой (SC) - самый внешний слой кожи, защищает организм от внешних агентов и контролирует обмены с окружающей средой, особенно трансэпителиальную потерю воды (TEWL). Структурная организация рогового слоя и присутствие гигроскопичных молекул, вместе называемых NMF, позволяют роговому слою удерживать воду, таким образом сохраняя эпидермис увлажненным и эластичным. Роговой слой состоит из окончательно дифференцированных кератиноцитов, называемых корнеоцитами, которые расположены в плотными слоями и объединены корнеодесмосомами. Корнеоциты встроены в гидрофобный липидный внеклеточный матрикс, ороговевшую клеточную оболочку (Pouillot, Dayan, Polla, Polla, & Polla, 2008). Хотя барьер, создаваемый роговым слоем, по своей структуре напоминает кирпичную стену, он имеет более динамичный и сложный характер (Elias, 1983). Фактически, ороговевшая клеточная оболочка, окружающая неделящиеся заполненные кератином корнеоциты, представляет собой активную среду, состоящую из ферментов, участвующих в дифференцировке эпидермиса и формировании NMF (Pouillot et al., 2008).
Соответствующий уровень гидратации необходим для поддержания механических свойств кожи, таких как прочность, гибкость и эластичность (Mojumdar, Pham, Topgaard, & Sparr, 2017). In vivo нормальный уровень гидратации находится в диапазоне 30–50% от сухого веса рогового слоя (Caspers, Lucassen, Carter, Bruining, & Puppels, 2001). Вода, обнаруживаемая в роговом слое, в основном поглощается корнеоцитами, способными увеличивать свой вес при набухании до 50% (Richter, Müller, Schwarz, Wepf, & Wiesendanger, 2001; Mojumdar et al., 2017). В условиях низкой относительной влажности (RH) роговой слой является хрупким и ломким, становясь более эластичным по мере увеличения относительной влажности (Mojumdar et al., 2017). Изменения относительной влажности также изменяют подвижность кератиновых нитей, присутствующих в корнеоцитах, подтверждая тем самым роль воды в пластификации кератина (Mojumdar et al., 2017).
NMF имеет решающее значение для поддержания здорового рогового слоя, поскольку играет важную роль в увлажнении кожи (Robinson, Visscher, Laruffa, & Wickett, 2010). Снижение уровня NMF вызывает потерю воды в роговом слое и снижает эластичность эпидермиса (Verdier-Sévrain & Bonté, 2007). NMF состоит из молекул, которые образуются в результате распада белков или секретируются сальными и потовыми железами. Подробный состав NMF изображен на рисунке 1. Разложение филаггрина, кератин-агрегирующего белка оболочки ороговевших клеток, который образуется во время дифференцировки кератиноцитов (Simon et al., 1996; Kezic, Kammeyer, Calkoen, Fluhr, & Bos, 2009), приводит к образованию гигроскопичных аминокислот и других побочных продуктов, включая мочевину (Björklund et al., 2014). В здоровом роговом слое мочевине соответствует 7% NMF, процент, который снижается с возрастом (Verdier-Sévrain & Bonté, 2007).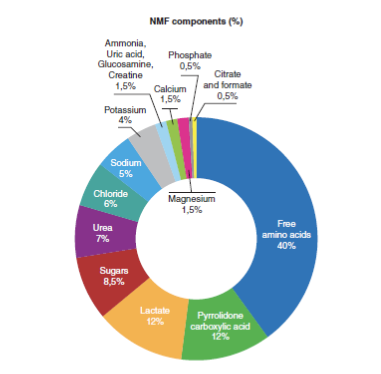
Компоненты NMF (%)
По часовой стрелке: свободные аминокислоты; пирролидонкарбоновая кислота; лактат; сахара; мочевина; хлориды; натрий; калий; аммиак, мочевая кислота, глюкозамин, креатинин; кальций; фосфаты; цитрат и формиат.
РИСУНОК 1 Химический состав NMF. Данные из (Verdier-Sévrain & Bonté, 2007 г.)
МОЧЕВИНА И ФУНКЦИОНАЛЬНАЯ ЦЕЛОСТНОСТЬ МОЗОЛИСТОГО СЛОЯ
На протяжении многих лет увлажняющее действие мочевины исследовалось in vivo (Serup, 1992; Bettinger, Gloor, Gehring, & Wolf, 1995; Treffel & Gabard, 1995; Loden, 1996, 1997; Kuzmina, Hagströmer, & Emtestam, 2002); Grether-Beck, Mühlberg, Brenden, & Krutmann, 2008; Borelli, Bielfeldt, Borelli, Schaller, & Korting, 2011). Пан и его коллеги проанализировали эти клинические данные в 2013 году (Pan, Heinecke, Bernardo, Tsui, & Levitt, 2013). Было отмечено, что мочевина снижает трансэпидермальную потерю воды (Loden, 1996, 1997; Borelli et al., 2011), улучшает гидратацию (Borelli et al., 2011) и удерживает воду (Treffel & Gabard, 1995). Кроме того, мочевина способна увеличивать количество свободной воды в условиях высокой влажности (Bettinger et al., 1995) и действовать как мощный увлажнитель кожи и отшелушивающее средство (Serup, 1992).
Следует отметить тот факт, что во всех указанных клинических исследованиях использовались составы для местного применения в виде крема, эмульсии или пены с концентрацией мочевины 10% или меньше. О нежелательных явлениях не сообщалось, что подтверждает безопасность применения препаратов на основе мочевины для местного применения.
Мочевина увеличивает содержание воды в роговом слое, действуя как увлажнитель, но также за счет сохранения текучести рогового слоя (Albèr et al., 2014; Mojumdar et al., 2017). Путём измерения корнеометрии, Albèr et al. обнаружили, что мочевина способствует увлажнению кожи даже при применении в составе с пониженной водной активностью (Albèr et al., 2014). В последующем исследовании изучались молекулярные характеристики кератина и макроскопические свойства рогового слоя (SC) после добавления мочевины к дегидратированным SC и корнеоцитам, и было обнаружено, что изменения были аналогичны изменениям, происходящим при увеличении относительной влажности в отсутствие мочевины (Mojumdar et al., 2017). Эти данные подтверждают гипотезу о том, что мочевина действует как естественный эндогенный увлажнитель, заменяя воду в условиях низкой влажности и поддерживая уровень жидкости в составе рогового слоя (Mojumdar et al., 2017). В более высоких концентрациях (>10%) (например, Аквапилинг (aquapiling.net)) мочевина оказывает смягчающее/кератолитическое действие. Первые доказательства были получены в исследованиях Суонбека в 60-х годах. Эти исследования показали, что препараты с высокой концентрацией мочевины можно использовать для лечения ихтиоза и других гиперкератозных состояний (Swanbeck, 1968a, 1968b; Swanbeck & Rajka, 1970). Суонбек предположил, что при высоких концентрациях мочевина способна растворять кератин, способствуя разрушению водородных связей. Дальнейшие исследования показали, что мочевина способна вызывать конформационные изменения кератина, вызывающие денатурацию белковой структуры (Pan et al., 2013).
Помимо свойств увлажнения, сохранения текучести SK и активизации денатурации кератина, мочевина также способна участвовать в регуляции экспрессии генов (Friedman, von Grote, & Meckfessel, 2016). В исследовании Grether-Beck et al. указывается на, что мочевина индуцирует экспрессию эпидермальных генов (Grether-Beck et al., 2012). Хотя необходимы дополнительные исследования для лучшего понимания участия мочевины в регуляции экспрессии генов в SK, активная роль мочевины как индуктора экспрессии эпидермальных генов может объяснить положительные эффекты мочевины в сохранении функции кожного барьера.
МОЧЕВИНА И ЛЕЧЕНИЕ ДЕРМАТОЛОГИЧЕСКИХ СОСТОЯНИЙ
Нарушения кератинизации характеризуются качественными или количественными изменениями структуры рогового слоя. Мочевина, используемая отдельно или в комбинированной терапии, улучшает лечение таких патологических состояний, включая ксероз, атопический дерматит, вульгарный ихтиоз, псориаз и онихомикоз (Pan et al., 2013).
Ксероз или сухость кожи может быть результатом обезвоживания или изменения выработки липидов. Обезвоженная кожа, типичная для пожилых людей, в тканях которых отсутствует вода – тонкая, слабая и хрупкая. Низкое количество кожного сала и аномальные уровни липидов в эпидермисе (как при атопическом дерматите) делают кожу нежной, непрозрачной, красной и гиперчувствительной к внешним агентам. В обоих случаях составы для местного применения, содержащие мочевину, играют важную роль в лечении заболеваний. При использовании в низких дозах (в основном <10%, в одном исследовании использовалось 40% мочевины) мочевина регулирует трансэпидермальную потерю воды (TEWL) и восстанавливает способность рогового слоя мобилизовать и поддерживать гидратацию (Pan et al., 2013; Danby et al., 2016). Увлажняющие средства, содержащие мочевину, улучшают заживление трещин у пациентов с диабетом (Federici, Federici, & Milani, 2015; Gin et al., 2017). Открытые пяточные трещины позволяют бактериям проникать внутрь и могут привести к инфекциям и дальнейшим осложнениям. Кроме того, процедура ухода за кожей, включающая этап увлажнения, останавливает прогрессирование заболеваний сухой кожи, включая гиперпролиферацию эпидермиса и воспаление (Friedman, von Grote, & Meckfessel, 2016).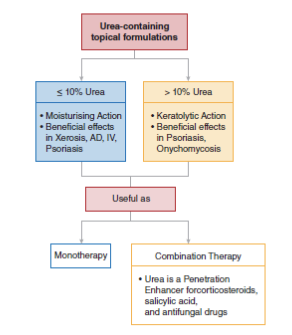
Сверху вниз, слева направо: составы с мочевиной для местного применения; ≤10% мочевины, увлажняющее действие, положительное действие при ксерозе, AД, IV, псориазе; ≥10% мочевины, кератолитическое действие, положительное действие при псориазе, онихомикозе; полезна в качестве; монотерапия; комбинированная терапия, мочевина – усилитель проникновения кортикостероидов, салициловой кислоты и противогрибковых препаратов.
РИСУНОК 2 Обзор известных эффектов препаратов для местного применения, содержащих мочевину, в клинических условиях. AД, топический дерматит; IV, вульгарный ихтиоз
Дисфункцию кожного барьера связывают с повышенным риском развития атопического дерматита (АД) (Egawa & Kabashima, 2018). Ослабленный кожный барьер облегчает проникновение аллергенов и других внешних агентов и предрасполагает организм к воспалению. Если воспаление кожи не проходит, барьерная функция нарушается еще больше (Egawa & Kabashima, 2018). АД является наиболее распространенным воспалительным заболеванием кожи, которым страдают до 30% детей во всем мире (Bieber, 2008). АД является кожным проявлением генетической предрасположенности к аллергии и характеризуется очень зудящими и рецидивирующими кожными поражениями на сухой коже (Egawa & Kabashima, 2018). Соответствующая гидратация рогового слоя кажется крайне важной при предотвращении АД, поскольку применение увлажняющих кремов у новорожденных снижает распространенность заболевания (Horimukai et al., 2014; Simpson et al., 2014).
В нескольких клинических испытаниях изучались клинические эффекты содержащих мочевину препаратов для местного применения при АД (Pan et al., 2013). Было установлено, что при концентрации 10% мочевина улучшает гидратацию кожи и снижает трансэпидермальную потерю воды (TEWL) у пациентов с АД (Sasaki, Tadaki, & Tagami, 1989). При этом в двух недавних исследованиях утверждается, что мочевина усиливает гидратацию кожи при АД без снижения TEWL (Hoppe et al., 2015; Ahmad Nasrollahi et al., 2018). Данные противоречивые результаты можно объяснить низкой концентрацией мочевины, используемой в применяемых составах (всего 5%).
Клиническое преимущество мочевины при АД наблюдалось при использовании отдельно и в комбинации с гидрокортизоном или валератом бетаметазона-17 (Bohnsack, Tausch, Gassmuller, & Rippke, 1997; Wilhelm, Scholermann, & Bohnsack, 1998; Loden et al., 2002; Wirén. et al., 2009; Pan et al., 2013). Следует отметить, что комбинированная терапия с мочевиной оказалась более эффективной, чем лечение только гидрокортизоном или бетаметазон-17-валератом (Pan et al., 2013). Недавний Кокрановский обзор подтвердил, что при АД лечение увлажняющими средствами и местными кортикостероидами более эффективно, чем лечение только местными кортикостероидами (Van Zuuren, Fedorowicz, & Arents, 2017). Систематический обзор подтвердил положительный эффект увлажняющих средств при АД, но предупредил о необходимости проведения более узко специализированных исследований, которые позволили бы проводить прямые сравнения увлажняющих средств (Lindh & Bradley, 2015). Между тем, имеющиеся данные подтверждают использование увлажняющих средств, содержащих мочевину, в качестве терапии первой линии при АД (Lindh & Bradley, 2015).
Вульгарный ихтиоз (IV) – это генетическое заболевание с распространенностью 1:300, вызванное мутациями с потерей функции в гене филаггрина (FLG) (Brown & McLean, 2012). IV характеризуется шелушащейся сухой кожей с симметричными белыми или серыми чешуйками. Шелушение происходит из-за отсутствия белка филаггрина в роговом слое, что вызывает низкую клеточную регенерацию рогового слоя и хроническое накопление кератина. В недавнем систематическом обзоре сделан вывод о том, что препараты, содержащие мочевину, следует использовать в качестве терапии первой линии при вульгарном ихтиозе (Lindh & Bradley, 2015). Поддерживающая терапия с использованием 10% мочевины ничем не хуже терапии, содержащей 1% гидрокортизон, 2% салициловую кислоту или парафиновые увлажнители (Pan et al., 2013).
Псориаз – хроническое воспалительное заболевание кожи, распространенность которого во всем мире составляет 2% (Parisi, Symmons, Griffiths, & Ashcroft, 2013). Псориаз характеризуется развитием эритематозных шелушащихся бляшек, которые возникают в результате усиленной пролиферации кератиноцитов и измененной дифференцировки эпидермиса (Zhang et al., 2009). Были проведены клинические испытания для изучения влияния мочевины на псориатическую кожу (Pan et al., 2013). В одном из исследований было установлено, что при использовании в концентрации 10% мочевина снижает трансэпидермальную потерю воды (TEWL) и усиливает гидратацию рогового слоя (Sasaki, Tadaki, & Tagami, 1989). Впоследствии Хагеманн и Прокш также обнаружили, что мочевина вызывает дифференцировку эпидермиса (Hagemann & Proksch, 1996). При использовании в концентрации от 10 до 40%, отдельно или в комбинации с бифоназолом или дитранолом, в большинстве исследований сообщалось об улучшении отшелушивания и клинического состояния у пациентов с псориазом (Pan et al., 2013). (например, Аквапилинг (aquapiling.net))
В концентрации 40% мочевина демонстрирует клиническое действие при лечении грибковых инфекций ногтей, таких как онихомикоз (Pan et al., 2013). Местное лечение флуконазолом 1% и мочевиной 40% более эффективно, чем одним флуконазолом при лечении онихомикоза (Bassiri-Jahromi, Ehsani, Mirshams-Shahshahani, & Jamshidi, 2012). Мочевина усиливает проникновение противогрибкового агента и, таким образом, усиливает лечебный эффект (Pan et al., 2013). (например, Крем-паста от натоптышей Аквапилинг (aquapiling.net))
Мочевина может считаться усилителем проникновения в силу своей способности облегчать транспорт потока молекул через ноготь и кожу (Trommer & Neubert, 2006). Данные молекулы включают вышеупомянутые противогрибковые препараты, а также другие соединения, используемые при лечении кожных заболеваний, такие как кортикостероиды (Trommer & Neubert, 2006). В более раннем исследовании Эйреса и Хупера изучалось усиливающее действие мочевины при проникновении кортизола через кожу (Ayres & Hooper, 1978). Авторы заметили, что препарат для местного применения, содержащий 1,0% кортизола и 10% мочевины, доставлял в кожу в восемь раз больше кортизола, чем крем для местного применения, использованный в качестве контроля (1,0% кортизола в креме, смешиваемым с водой). Последующие исследования показали, что мочевина усиливает проникновение гидрокортизона, прогестерона и лейпролида через подкожную клетчатку (Trommer & Neubert, 2006). Следует отметить, что в исследовании in vitro, в котором изучалась чрескожная диффузия прогестерона, мочевина увеличивала проникновение прогестерона в 2,5 раза (Valenta & Wedenig, 1997).
Механизм, с помощью которого мочевина увеличивает проницаемость рогового слоя, полностью не изучен, но считается, что он связан со способностью увеличивать содержание воды, абсорбированной корнеоцитами, что является прямым следствием высокой способности связывать воду (Mueller et al., 2016). В более высоких дозах кератолитическое действие мочевины также может играть роль в усилении проникновения лекарственных средств (Trommer & Neubert, 2006). Вследствие признанного действия в качестве химического усилителя проникновения мочевину следует использовать вместе с местными кортикостероидами, салициловой кислотой или противогрибковыми препаратами для улучшения доставки лекарств и результатов лечения.
ВЫВОД
Мочевина – хорошо известное увлажняющее и кератолитическое средство. Мочевина уже более века безопасно используется для поддержания здоровья кожи и лечения ряда кожных заболеваний. Клинические исследования подтвердили положительное действие мочевины при заболеваниях, связанных с дисфункцией кожного барьера. При использовании в разных концентрациях мочевина оказывает разное действие (рис. 2). Более низкую концентрацию мочевины (≤10%) связывают с увлажняющим эффектом, тогда как более высокая концентрация (>10%) оказывает смягчающее/кератолитическое действие. Как усилитель проникновения через кожу мочевина облегчает пересечение кожного барьера другими молекулами и, таким образом, улучшает действие лекарств, используемых в комбинированной терапии. Составы для местного применения, содержащие мочевину, доступны в различных концентрациях и предоставляют врачам широкий спектр альтернатив для повышения эффективности лечения кожных заболеваний и улучшения самочувствия пациента.
БЛАГОДАРНОСТЬ
Поддержка по составлению и редактированию медицинских текстов была предоставлена Ракель Карвалхоса, доктором философии, и компанией «ЭРА МС СРЛ (ERA MS SRL)». Финансовую поддержку при составлении и редактировании медицинских текстов оказала компания «РЕЛАЙФ СРЛ (RELIFE SRL)».
КОНФЛИКТ ИНТЕРЕСОВ
Авторы заявляют об отсутствии конфликта интересов.
ORCID Леонардо Челлено https://orcid.org/0000-0002-7129-198X
ИСПОЛЬЗОВАННАЯ ЛИТЕРАТУРА
Ahmad Nasrollahi, S., Ayatollahi, A., Yazdanparast, T., Samadi, A., Hosseini, H., Shamsipour, M., … Firooz, A. (2018). Comparison of linoleic acid-containing water-in-oil emulsion with urea-containing water-in-oil emulsion in the treatment of atopic dermatitis: A randomized clinical trial. Clinical Cosmetic and Investigational Dermatology, 11, 21–28. https://doi.org/10.2147/CCID.S145561 Albèr, C., Buraczewska-Norin, I., Kocherbitov, V., Saleem, S., Lodén, M., & Engblom, J. (2014). Effects of water activity and low molecular weight humectants on skin permeability and hydration dynamics - a double-blind, randomized and controlled study. International Journal of Cosmetic Science, 36(5), 412–418. https://doi.org/10.1111/ics.12136 Ayres, P. J., & Hooper, G. (1978). Assessment of the skin penetration properties of different carrier vehicles for topically applied cortisol. British Journal of Dermatology, 99(3), 307–317. https://doi.org/10.1111/j. 1365-2133.1978.tb02002.x Bassiri-Jahromi, S., Ehsani, A. H., Mirshams-Shahshahani, M., & Jamshidi, B. (2012). A comparative evaluation of combination therapy of fluconazole 1% and urea 40% compared with fluconazole 1% alone in a nail lacquer for treatment of onychomycosis: Therapeutic trial. Journal of Dermatological Treatment, 23(6), 453–456. https://doi. org/10.3109/09546634.2011.588191 Bettinger, J., Gloor, M., Gehring, W., & Wolf, W. (1995). Influence of emulsions with and without urea on water-binding capacity of the stratum corneum. Journal of the Society of Cosmetic Chemists, 46(5), 247–254. Bieber, T. (2008). Atopic dermatitis. New England Journal of Medicine, 358(14), 1483–1494. https://doi.org/10.1056/NEJMra074081 Björklund, S., Andersson, J. M., Pham, Q. D., Nowacka, A., Topgaard, D., & Sparr, E. (2014). Stratum corneum molecular mobility in the presence of natural moisturizers. Soft Matter, 10(25), 4535–4546. https://doi. org/10.1039/C4SM00137K Bohnsack, K., Tausch, I., Gassmuller, J., & Rippke, F. (1997). Efficacy on the symptom “dry skin” and long-term dermal tolerance of Laceran lotion 10% urea in patients with atopic dermatitis. Zeitschrift für Hautkrankheiten, 72, 34–39. Borelli, C., Bielfeldt, S., Borelli, S., Schaller, M., & Korting, H. C. (2011). Cream or foam in pedal skin care: Towards the ideal vehicle for urea used against dry skin. International Journal of Cosmetic Science, 33(1), 37–43. https://doi.org/10.1111/j.1468-2494.2010.00576.x Brown, S. J., & McLean, W. H. I. (2012). One remarkable molecule: filaggrin. The Journal of Investigative Dermatology, 132(3 Pt 2), 751–762. https://doi.org/10.1038/jid.2011.393 Caspers, P. J., Lucassen, G. W., Carter, E. A., Bruining, H. A., & Puppels, G. J. (2001). In vivo confocal Raman microspectroscopy of the skin: Noninvasive determination of molecular concentration profiles. The Journal of Investigative Dermatology, 116(3), 434–442. https://doi. org/10.1046/j.1523-1747.2001.01258.x Danby, S. G., Brown, K., Higgs-Bayliss, T., Chittock, J., Albenali, L., & Cork, M. J. (2016). The effect of an emollient containing urea, ceramide NP, and lactate on skin barrier structure and function in older people with dry skin. Skin Pharmacology and Physiology, 29(3), 135–147. https://doi.org/10.1159/000445955 Egawa, G., & Kabashima, K. (2018). Barrier dysfunction in the skin allergy. Allergology International, 67(1), 3–11. https://doi.org/10.1016/j.alit. 2017.10.002 Elias, P. M. (1983). Epidermal lipids, barrier function, and desquamation. The Journal of Investigative Dermatology, 80(Suppl), 44s–49s. Federici, A., Federici, G., & Milani, M. (2015). Use of a urea, arginine and carnosine cream versus a standard emollient glycerol cream for treatment of severe xerosis of the feet in patients with type 2 diabetes: A randomized, 8 month, assessor-blinded, controlled trial. Current Medical Research and Opinion, 31(6), 1063–1069. https://doi.org/10. 1185/03007995.2015.1037731 Friedman, A. J., von Grote, E. C., & Meckfessel, M. H. (2016). Urea: A clinically oriented overview from bench to bedside. Journal of Drugs in Dermatology: JDD, 15(5), 633–639. Gin, H., Rorive, M., Gautier, S., Condomines, M., Saint Aroman, M., & Garrigue, E. (2017). Treatment by a moisturizer of xerosis and cracks of the feet in men and women with diabetes: A randomized, double-blind, placebo-controlled study. Diabetic Medicine, 34(9), 1309–1317. https://doi.org/10.1111/dme.13402 Grether-Beck, S., Felsner, I., Brenden, H., Kohne, Z., Majora, M., Marini, A., … Krutmann, J. (2012). Urea uptake enhances barrier function and antimicrobial defense in humans by regulating epidermal gene expression. Journal of Investigative Dermatology, 132(6), 1561–1572. https://doi. org/10.1038/jid.2012.42 Grether-Beck, S., Mühlberg, K., Brenden, H., & Krutmann, J. (2008). Urea plus ceramides and vitamins: Improving the efficacy of a topical urea preparation by addition of ceramides and vitamins. Der Hautarzt; Zeitschrift Fur Dermatologie, Venerologie, Und Verwandte Gebiete, 59(9), 717–718, 720–723. https://doi.org/10.1007/s00105-008-1594-z Hagemann, I., & Proksch, E. (1996). Topical treatment by urea reduces epidermal hyperproliferation and induces differentiation in psoriasis. Acta Dermato-Venereologica, 76(5), 353–356. Hoppe, T., Winge, M. C. G., Bradley, M., Nordenskjöld, M., Vahlquist, A., Törmä, H., & Berne, B. (2015). Moisturizing treatment of patients with atopic dermatitis and ichthyosis vulgaris improves dry skin, but has a modest effect on gene expression regardless of FLG genotype. Journal of the European Academy of Dermatology and Venereology, 29(1), 174–177. https://doi.org/10.1111/jdv.12333 Horimukai, K., Morita, K., Narita, M., Kondo, M., Kitazawa, H., Nozaki, M., … Ohya, Y. (2014). Application of moisturizer to neonates prevents development of atopic dermatitis. The Journal of Allergy and Clinical Immunology, 134(4), 824–830.e6. https://doi.org/10.1016/j.jaci.2014.07.060 Kapuscinska, A., & Nowak, I. (2014). The use of urea and its derivatives in the cosmetics industry. CHEMIK, 68(2), 91–98. Kezic, S., Kammeyer, A., Calkoen, F., Fluhr, J. W., & Bos, J. D. (2009). Natural moisturizing factor components in the stratum corneum as biomarkers of filaggrin genotype: Evaluation of minimally invasive methods. British Journal of Dermatology, 161(5), 1098–1104. https:// doi.org/10.1111/j.1365-2133.2009.09342.x Kuzmina, N., Hagströmer, L., & Emtestam, L. (2002). Urea and sodium chloride in moisturisers for skin of the elderly--a comparative, double-blind, randomised study. Skin Pharmacology and Applied Skin Physiology, 15(3), 166–174. https://doi.org/10.1159/000063545 Lindh, J. D., & Bradley, M. (2015). Clinical effectiveness of moisturizers in atopic dermatitis and related disorders: A systematic review. American Journal of Clinical Dermatology, 16(5), 341–359. https://doi.org/10. 1007/s40257-015-0146-4 Loden, M. (1996). Urea-containing moisturizers influence barrier properties of normal skin. Archives of Dermatological Research, 288(2), 103–107. Loden, M. (1997). Barrier recovery and influence of irritant stimuli in skin treated with a moisturizing cream. Contact Dermatitis, 36(5), 256–260. Loden, M., Andersson, A.-C., Anderson, C., Bergbrant, I.-M., Frödin, T., Ohman, H., … Lindberg, M. (2002). A double-blind study comparing the effect of glycerin and urea on dry, eczematous skin in atopic patients. Acta Dermato-Venereologica, 82(1), 45–47. Mojumdar, E. H., Pham, Q. D., Topgaard, D., & Sparr, E. (2017). Skin hydration: Interplay between molecular dynamics, structure and water uptake in the stratum corneum. Scientific Reports, 7(1), 15712. https:// doi.org/10.1038/s41598-017-15921-5 Mosher, H. H. (1933). Simultaneous study of constituents of urine and perspiration. Journal of Biological Chemistry, 99, 781. Mueller, J., Oliveira, J. S. L., Barker, R., Trapp, M., Schroeter, A., Brezesinski, G., & Neubert, R. H. H. (2016). The effect of urea and taurine as hydrophilic penetration enhancers on stratum corneum lipid models. Biochimica et Biophysica Acta (BBA) - Biomembranes, 1858(9), 2006–2018. https://doi.org/10.1016/j.bbamem.2016.05.010 Pan, M., Heinecke, G., Bernardo, S., Tsui, C., & Levitt, J. (2013). Urea: A comprehensive review of the clinical literature. Dermatology Online Journal, 19(11), 20392. Parisi, R., Symmons, D. P. M., Griffiths, C. E. M., & Ashcroft, D. M. (2013). Global epidemiology of psoriasis: A systematic review of incidence and prevalence. Journal of Investigative Dermatology, 133(2), 377–385. https://doi.org/10.1038/jid.2012.339 Pouillot, A., Dayan, N., Polla, A. S., Polla, L. L., & Polla, B. S. (2008). The stratum corneum: A double paradox. Journal of Cosmetic Dermatology, 7(2), 143–148. https://doi.org/10.1111/j.1473-2165.2008.00379.x Richter, T., Müller, J. H., Schwarz, U. D., Wepf, R., & Wiesendanger, R. (2001). Investigation of the swelling of human skin cells in liquid media by tapping mode scanning force microscopy. Applied Physics A, 72(S1), S125–S128. https://doi.org/10.1007/s003390100750 Robinson, M., Visscher, M., Laruffa, A., & Wickett, R. (2010). Natural moisturizing factors (NMF) in the stratum corneum (SC). I. Effects of lipid extraction and soaking. Journal of Cosmetic Science, 61(1), 13–22. Sasaki, Y., Tadaki, T., & Tagami, H. (1989). The effects of topical application of urea cream on the function of pathological stratum corneum. Acta Dermatol-Kyoto, 84(4), 581–586. Serup, J. (1992). A three-hour test for rapid comparison of effects of moisturizers and active constituents (urea). Measurement of hydration, scaling and skin surface lipidization by noninvasive techniques. Acta Dermato-Venereologica. Supplementum, 177, 29–33. Simon, M., Haftek, M., Sebbag, M., MontéZin, M., Girbal-Neuhauser, E., Schmitt, D., & Serre, G. (1996). Evidence that filaggrin is a component of cornified cell envelopes in human plantar epidermis. Biochemical Journal, 317(1), 173–177. https://doi.org/10.1042/bj3170173 Simpson, E. L., Chalmers, J. R., Hanifin, J. M., Thomas, K. S., Cork, M. J., McLean, W. H. I., … Williams, H. C. (2014). Emollient enhancement of the skin barrier from birth offers effective atopic dermatitis prevention. Journal of Allergy and Clinical Immunology, 134(4), 818–823. https:// doi.org/10.1016/j.jaci.2014.08.005 Swanbeck, G. (1968a). A new treatment of ichthyosis and other hyperkeratotic conditions. Acta Dermato-Venereologica, 48(2), 123–127. Swanbeck, G. (1968b). Carbamide cream for dry and hyperkeratotic skin. Läkartidningen, 65(22), 2286–2290. Swanbeck, G., & Rajka, G. (1970). Antipruritic effect of urea solutions. An experimental and clinical study. Acta Dermato-Venereologica, 50(3), 225–227. Treffel, P., & Gabard, B. (1995). Stratum corneum dynamic function measurements after moisturizer or irritant application. Archives of Dermatological Research, 287(5), 474–479. Trommer, H., & Neubert, R. H. (2006). Overcoming the stratum corneum: The modulation of skin penetration. A review. Skin Pharmacology and Physiology, 19(2), 106–121. https://doi.org/10.1159/000091978 Valenta, C., & Wedenig, S. (1997). Effects of penetration enhancers on the in-vitro percutaneous absorption of progesterone. Journal of Pharmacy and Pharmacology, 49(10), 955–959. https://doi.org/10.1111/j.2042-7158. 1997.tb06023.x Van Zuuren, E. J., Fedorowicz, Z., & Arents, B. W. M. (2017). Emollients and moisturizers for eczema: Abridged Cochrane systematic review including GRADE assessments. British Journal of Dermatology, 177(5), 1256–1271. https://doi.org/10.1111/bjd.15602 Verdier-Sévrain, S., & Bonté, F. (2007). Skin hydration: A review on its molecular mechanisms. Journal of Cosmetic Dermatology, 6(2), 75–82. https://doi.org/10.1111/j.1473-2165.2007.00300.x Wilhelm, K. P., Scholermann, A., & Bohnsack, K. (1998). Efficacy and tolerability of a topical preparation containing 10% urea in patients with atopic dermatitis. Aktuelle Dermatologie, 24, 26–30. Wirén, K., Nohlgård, C., Nyberg, F., Holm, L., Svensson, M., Johannesson, A., … Lodén, M. (2009). Treatment with a barrier-strengthening moisturizing cream delays relapse of atopic dermatitis: A prospective and randomized controlled clinical trial. Journal of the European Academy of Dermatology and Venereology, 23(11), 1267–1272. https://doi.org/10. 1111/j.1468-3083.2009.03303.x Zhang, X.-J., Huang, W., Yang, S., Sun, L.-D., Zhang, F.-Y., Zhu, Q.-X., … Liu, J.-J. (2009). Psoriasis genome-wide association study identifies susceptibility variants within LCE gene cluster at 1q21. Nature Genetics, 41(2), 205–210. https://doi.org/10.1038/ng.31