Повышение эффективности лечения детей с атопическим дерматитом
А.В. Камаев1, О.В. Трусова1, У.А. Бутырина2, И.В. Макарова1
1ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. академика И.П. Павлова» Минздрава России, Санкт-Петербург, Россия;
2Детское поликлиническое отделение №60 Городской поликлиники №91, Санкт-Петербург, Россия
Активные исследования атопического дерматита выявляют новые звенья патогенеза и подтверждают необходимость комплексного подхода к лечению, включающего различные формы выпуска увлажняющих препаратов (крем и средство для купания).
Цель исследования: показать эффективность комбинации увлажняющего крема и средства для купания отечественного производства (марка «Липобейз baby») в комплексном лечении детей раннего возраста с атопическим дерматитом.
Пациенты и методы. В открытое проспективное несравнительное исследование продолжительностью 30 дней включены 30 детей (60% мальчики) в возрасте от 6 до 36 мес со среднетяжелым/легким атопическим дерматитом. На каждом визите (дважды через 2 нед) врач рассчитывал индекс SCORAD и собирал дневники ежедневного учета выраженности зуда кожи и нарушений сна, использования препаратов и нежелательных явлений. Дополнительно оценивали общее впечатление врача от проведенного лечения (индекс GETE).
Результаты. Средний комплайенс пациентов по использованию увлажняющих препаратов составил 89,2% дней. Средние значения индекса SCORAD снижались по визитам: 23,5±7,3, 18,7±4,9 и 14,6±3,1 балла. Через 2 нед применения увлажняющие средства значительно снижали выраженность зуда (с 6,4 до 3,6 балла) и связанные с ним нарушения сна ребенка (с 2,6 до 1,2 балла). Выявлена прямая умеренная связь (r=0,64; р=0,012) между числом дней без зуда кожи или нарушений сна и компла-йенсом использования увлажняющей косметики. Связанных с препаратами нежелательных явлений не зарегистрировано.
Заключение. Включение в комплексную терапию атопического дерматита увлажняющего крема и средства для купания отечественного производства (марка «Липобейз baby») повышает эффективность лечения.
Ключевые слова: дети, атопический дерматит, эмолиенты, эффективность лечения.
Для цитирования: Камаев А.В., Трусова О.В., Бутырина У.А., Макарова И.В. Повышение эффективности лечения детей с атопическим дерматитом в результате использования комплекса эмолиентов. Рос вестн перинатол и педиатр 2019; 64:(3): 109-117. DOI: 10.21508/1027-4065-2019-64-3-109-117
Проблема ведения пациентов с атопическим дерматитом привлекает внимание не только дерматологов и аллергологов-иммунологов, но и педиатров широкого профиля, а также врачей других специальностей. Как в отечественных, так и в более крупных международных эпидемиологических исследованиях на протяжении ближайших десятилетий отмечается рост распространенности этой нозологии, особенно среди детей первого года жизни [1—3]. Такая распространенность прямо определяет актуальность представления информации об алгоритмах диагностики и ведения педиатрических пациентов с атопическим дерматитом не только дерматологам или аллергологам-иммунологам, но и в первую очередь педиатрам широкого профиля.
Известные попытки первичной профилактики болезней атопического круга пока представляются безуспешными в глобальном плане. Растет распространенность не только атопического дерматита, но и аллергического ринита, и бронхиальной астмы у детей [4, 5]. Для аллерголога-иммунолога атопический дерматит в раннем возрасте может служить маркером повышенного риска формирования аллергического ринита и бронхиальной астмы у ребенка в будущем. Один из наиболее эффективных методов первичной профилактики дерматита и вторичной профилактики последующего движения ребенка по «атопическому маршу» в сторону респираторной аллергии — использование средств лечебной косметики [6].
Актуальная концепция патогенеза атопического дерматита в настоящее время предполагает равные и взаимодополняющие роли трех ключевых компонентов: пищевой сенсибилизации, межклеточных контактов эпидермиса (в частности, состоятельности филлагрина) и хронического иммунного воспаления кожи [7, 8]. Исходя из этого все современные руководства подчеркивают необходимость мотивации родителей на регулярное долгосрочное применение комплекса средств ухода за кожей — лечебной косметики наряду с активным использованием противовоспалительных средств (топических глюкокортикостероидов и топических ингибиторов кальциневрина). Такие средства лечебной косметики широко представлены различными производителями в аптечной сети; нередко выбор конкретной марки представляет затруднение не только для родителей пациента, но и для постоянно наблюдающего ребенка педиатра широкого профиля. Результаты исследований, проведенных с участием российских пациентов, могут служить одним из аргументов в пользу выбора лечебной косметики определенного производителя.
В отечественной педиатрической практике ранее широко была распространена рекомендация по ограничению в купании детей с атопическим дерматитом [9]; современные руководства и изменившиеся подходы к использованию нелекарственных средств ухода за кожей отвергают это положение [7, 10]. При условии использования прохладных (36—37 ) непродолжительных (до 10 мин) ванн с применением бесщелочных очищающих средств можно не только достичь дополнительной гидратации кожи ребенка, но и обеспечить лучший доступ лечебных и питательных средств для улучшения функций эпидермиса [11].
Настоящее исследование предпринято в условиях клинической практики для оценки эффективности комплекса средств ухода за кожей отечественного производства: увлажняющего и восстанавливающего крема и масла для купания «Липобейз baby» в ведении пациентов раннего возраста с атопическим дерматитом. По данным, представленным производителем, «Липобейз baby», крем для тела содержит физиологические натуральные масла (макадамии, оливковое, кокосовое, зародышей пшеницы) и обеспечивает кожу комплексом липидов, необходимых для восстановления и поддержания кожного барьера, питает и смягчает кожу, делает ее эластичной и гладкой. Другие компоненты крема оказывают увлажняющее (хлопковое молочко), регенерирующее (пантенол) и антиоксидантное (экстракт розмарина и витамин Е) действия.
Входящий в состав экстракт розмарина нормализует баланс микробиома кожи. Крем не содержит парабенов, минеральных масел, вазелина. В составе средства «Липобейз baby масло для купания» — масла макадамии, оливковое, миндальное и зародышей пшеницы. Эти компоненты бережно очищают кожу, восстанавливая и поддерживая ее барьерную функцию. Масло поддерживает баланс микробиома кожи благодаря экстракту розмарина и дает антиоксидантный эффект благодаря витамину Е.
Кроме того, представленная работа оценивает безопасность применения обсуждаемой гаммы косметических средств и удовлетворенность родителей использованием «Липобейз baby» в комплексном лечении атопического дерматита.
Характеристика детей и методы исследования
Исследование проведено на базе трех аллергологических кабинетов поликлинической сети г. Санкт-Петербурга: детского поликлинического отделения №41 городской поликлиники №44, детского поликлинического отделения №16 городской поликлиники №114, а также городского аллергокабинета детской городской поликлиники №44.
Дизайн протокола — открытое несравнительное проспективное исследование. В работу включены данные 30 пациентов, наблюдавшихся по поводу атопического дерматита в указанных поликлинических центрах. Продолжительность исследования — 30 дней, на протяжении которых каждый из включенных пациентов осуществил 3 визита с интервалом 14 дней (допускались отклонения от запланированной даты визита не более 2 дней). Препараты «Липобейз baby крем» и «Липобейз baby масло» для купания для пациентов на все время участия в исследовании предоставлены производителем — ООО «Фармтек». Частота визитов выбрана для оценки комплайенса в отношении использования средств лечебной косметики, а также для регистрации возможных нежелательных явлений. Применение увлажняющих препаратов осуществлялось согласно рекомендациям производителя: крема не реже чем 2 раза в день ежедневно, а масла для купания — через день для купания в большой ванне или ежедневно при использовании душа.
Для обеспечения соответствия клинической практике при отборе пациентов для участия в протоколе использован минимум критериев включения и невключения. К критериям включения относились:
— возраст от 6 до 35 мес;
— установленный не менее 1 мес перед включением диагноз атопического дерматита в соответствии с Федеральными клиническими рекомендациями [7];
— индекс SCORAD от 15 до 60 баллов.
Среди критериев невключения: нежелание сотрудничества в рамках протокола (частота визитов, заполнение дневника) у родителей пациента; известные анамнестические реакции на применение компонентов гаммы «Липобейз»; пиодермия или тяжелое, непрерывно-рецидивирующее течение, установленное при осмотре в день визита включения.
В качестве объективного инструмента оценки динамики патологического процесса при атопическом дерматите использовали индекс SCORAD, расчет которого проводили при включении в исследование и затем на каждом визите пациента в центр [12]. Кроме того, на визитах 2 и 3 наблюдающий врач аллерголог-иммунолог осуществлял общую оценку эффективности терапии (GETE index) в градациях оценки от «ухудшения», «состояния без перемен», до «улучшения» либо «выраженного улучшения» состояния пациента. К «улучшению» относили сохранение сухости кожи и высыпания при уменьшении их интенсивности и площади; к «выраженному улучшению» — отсутствие жалоб и объективных находок при осмотре.
Кроме индексов SCORAD и GETE, учитывали данные ежедневной субъективной оценки зуда кожи и нарушения сна из-за зуда кожи, отмечавшиеся родителями ежедневно в дневнике пациента. Для объективизации динамики у каждого пациента по данным показателям рассчитывали среднее значение на 1-4-й неделях, а затем полученные данные компоновали по всем включенным пациентам.
Зуд кожных покровов оценивали по визуальной аналоговой шкале (ВАШ) от 0 до 10 баллов: 0 баллов — отсутствие зуда, от 3 до 5 баллов — слабый зуд, от 6 до 8 баллов — умеренный зуд, от 9 до 10 баллов — тяжелый зуд. Нарушение сна также оценивали по ВАШ от 0 до 10 баллов, где 0 — отсутствует, 10 — сильно выражено. Отдельно учитывали число дней, в которые симптомы атопического дерматита нарастали (субъективное ухудшение), и число дней, когда пациентам потребовалось внепланово использовать противовоспалительный препарат (топические глюкокортикостероиды/топические ингибиторы кальциневрина, в зависимости от тяжести обострения). По данным дневников самонаблюдения, а также по результатам сбора анамнеза на визитах 2 и 3 определяли характер, частоту нежелательных явлений и их возможную связь с применением средств лечебной косметики.
Полученные результаты обрабатывали с использованием пакета StatisticaforWindows 10.0 («Statsoft Inc»., США). Данные представлены в виде среднего (М) и его стандартной ошибки (±а), в некоторых случаях — в виде медианы (Ме) с указанием первого и третьего квартилей [Q25; Q75]. Для оценки различий результатов выборок, учитывая вероятность отклонений от нормальности распределения, использовали непараметрический U-критерий Манна-Уитни. Различия считали статистически значимыми при р<0,05. При расчете корреляций в связи с оценкой связи между количественными и ранговыми показателями, а также небольшим объемом выборки использовали коэффициент Спирмена.
Результаты
В исследование включены 30 пациентов, в том числе 18 (60%)* мальчиков. Медиана возраста в выборке составила 13,6 мес, первый и третий квартили ([Q25; Q75]) - [7,2; 19,5] мес соответственно. Давность регистрации диагноза атопического дерматита преимущественно превышала 10 мес: медиана 10,6 [5,8; 15,4] мес.
Подгруппа легкого течения атопического дерматита состояла из 19 (63,3%) детей, подгруппа среднетяжелого течения - из 11 (36,7%). Для купирования обострений основным противовоспалительным средством были топические глюкокортикостероиды у 8 (26,7%) пациентов, топические ингибиторы кальци-неврина - у 15 (50%), у 7 (23,3%) детей обострения купировали без использования противовоспалительных средств (пероральные антигистаминные средства, препараты цинка, увеличение объема эмолиентов).
Четкая связь обострений с употреблением определенного пищевого продукта прослеживалась у 22 (73,3%) детей, у остальных причинами обострений были нарушения работы желудочно-кишечного тракта (как задержки, так и учащение/разжижение стула) — у 5 (16,7%) детей и ОРВИ — у 3 (10%). Среди пациентов с анамнестически очерченной пищевой сенсибилизацией ведущим аллергеном было коровье молоко (у 21 ребенка, или 95,4%), пшеница (у 10 детей, или 45,4%), белок куриного яйца (у 9 детей, или 40,9%) и овсяная крупа (у 7 детей, или 31,8%).
На визите 1 зарегистрировано обострение атопического дерматита у 18 (60%) больных, в том числе в подгруппе пациентов со среднетяжелым течением — у 7 (38,9%) и в подгруппе пациентов с легким течением заболевания — у 11 (61,1%). Всем детям, наряду с выдачей препаратов гаммы «Липобейз» назначены топические глюкокортикостероиды или топические ингибиторы кальциневрина в соответствии с общепринятой клинической практикой в зависимости от объема и выраженности зарегистрированных обострений на сроки от 5 до 10 дней. Из 30 детей 12 (40%) были включены в протокол в состоянии ремиссии, им выдавались письменные рекомендации по сочетанному применению средств лечебной косметики («Липобейз baby крем» и «Липобейз baby масло» для купания) и противовоспалительного средства (топические глюкокортикостероиды/топические ингибиторы кальциневрина) с первого дня обострения, в случае его развития вне сроков визита по протоколу.
Все пациенты, включенные в исследование, осуществили оба визита последующего наблюдения в запланированные протоколом сроки; анализируемая выборка для каждого из визитов составляет 30 пациентов.
К визиту 2 число пациентов, у которых зарегистрировано обострение атопического дерматита, уменьшилось до 7 (23,3%), в их числе: 5 (71,4%) из 19 детей со среднетяжелым течением и 2 (28,6%) из 11 — с легким течением болезни. К визиту 3 в состоянии обострения дерматита находились только 3 ребенка со среднетяжелым течением заболевания, у 2 из них это обострение было спровоцировано погрешностью в элиминационной диете в предшествовавшую визиту неделю — контактом с известным пищевым аллергеном.
Комплайенс в отношении использования препаратов (число дней применения «Липобейз baby крема» 2 раза и более, по данным дневников самонаблюдения) составил 100% у 25 (83,3%) детей к визиту 2; у остальных 5 детей он колебался от 85,8 до 92,9%. К визиту 3 доля пациентов, полностью выполнивших назначения врача, составила 80% (24 ребенка); еще 5 детей пропустили от одного до двух дней (комплайенс более 80%), один пациент пропустил 5 дней использования в связи с поездкой к бабушке (препарат забыли дома), однако это не привело к обострению атопического дерматита. Расход препаратов составил по одной упаковке каждого из средств в течение 12—16 дней, на всю продолжительность исследования — по две упаковки «Липобейз baby крема» и масла для купания на каждого пациента.
Исходно средний по группе индекс SCORAD составил 23,5±7,3 балла. В дальнейшем, к визиту 2 и особенно к визиту 3, средние значения индекса SCORAD неуклонно снижались (рис. 1). При сопоставлении результатов визита 1 и визита 3 оказалось, что снижение индекса SCORAD достигло статистической значимости (р=0,041). Это прямо связано с уменьшением числа пациентов в состоянии обострения дерматита.
Данные по разделению пациентов на подгруппы легкого и среднетяжелого течения атопического дерматита, а также по числу пациентов в состоянии обострения на каждый из визитов исследования и средним значениям индекса SCORAD (±с) по более мелким подгруппам представлены в сводной табл. 1.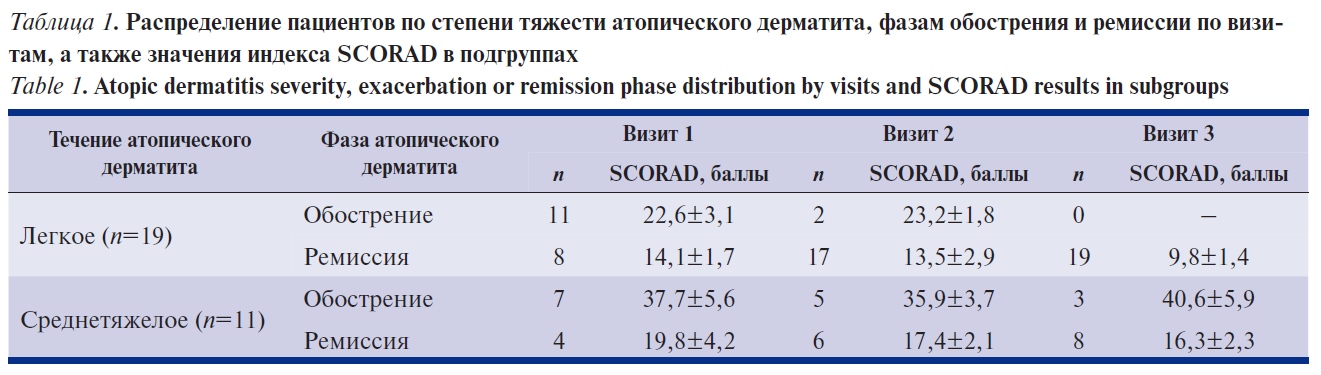
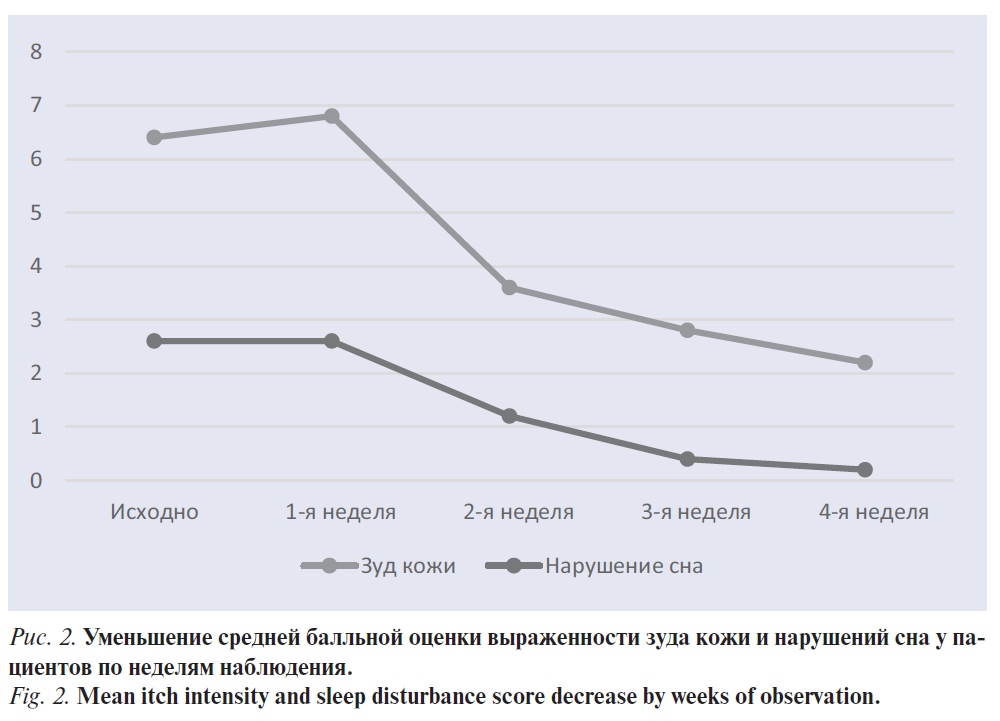
Как по суммарному индексу SCORAD, так и по отдельным субъективным показателям наиболее значимым для качества жизни ребенка с атопическим дерматитом и членов его семьи — зуду кожи и нарушению сна — наблюдалась отчетливая положительная динамика. Поскольку в отличие от характера и площади поражения кожи оба эти показателя всегда оцениваются родителями, в рамках настоящего исследования мы включили эти показатели в дневник самонаблюдения для ежедневной оценки. На рис. 2 представлены средние значения обоих показателей с недельными интервалами; статистически значимое снижение на фоне применения средств лечебной косметики «Липобейз baby крем» и «Липобейз baby масло» для купания наблюдалось уже после 2 нед использования препаратов.
Число дней, в которые пациенты не испытывали зуд кожи и/или нарушения сна, также значительно увеличивалось на протяжении регулярного применения средств лечебной косметики; лучших результатов здесь ожидаемо достигла подгруппа пациентов с легким течением заболевания, включенных в исследование вне стадии обострения. Более подробно данные представлены в табл. 2.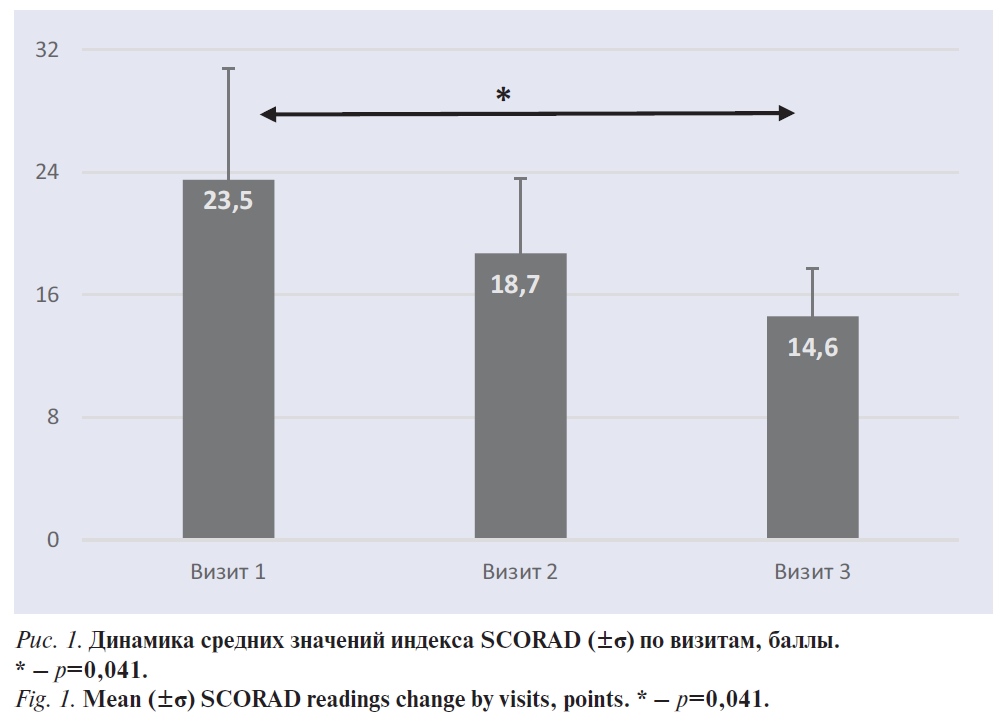
При расчете корреляции показателей «количество дней без зуда кожи либо нарушения сна» и комплайенса в отношении лечебной косметики по 3 рангам: полный, удовлетворительный (>80%) и неудовлетворительный (<80%) для всей выборки в целом получена умеренная прямая связь (r=0,64; р=0,012). Максимальной выраженности корреляция выявлена между показателями «использование масла для купания» (3 ранга: «ежедневное», «по рекомендациям (через день)» и «реже чем рекомендовано») и балльной оценкой зуда кожи — сильная обратная связь (r=—0,82; р=0,0001). Более подробно различные корреляции, выявленные в ходе настоящего исследования, представлены в табл. 3.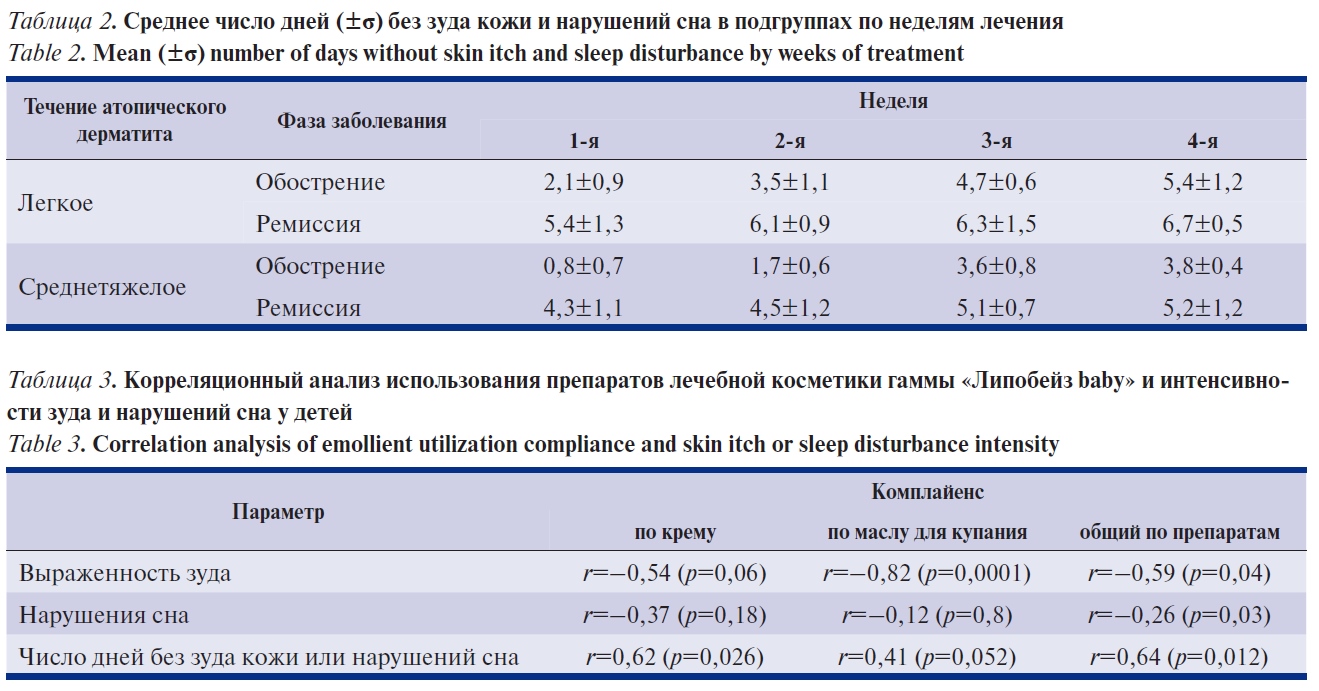
Как видно из данных, представленных в табл. 3, применение препаратов для восполнения липидов эпидермиса, восстановления барьерной функции кожи и ее дополнительного увлажнения уменьшает выраженность зуда кожи, нарушения сна у детей с атопическим дерматитом и повышает степень контроля заболевания в целом. Наблюдающие врачи отмечали только «улучшение» (8 пациентов, или 26,7%) либо «выраженное улучшение» (22 пациента, или 73,3%) в состоянии включенных пациентов. Даже у пациентов, у которых произошло обострение к моменту визита 3 (3 человека из группы среднетяжелого дерматита), общее впечатление от курса лечения в течение 30 дней расценено как «улучшение».
Не отмечено нежелательных реакций, связанных с использованием увлажняющего крема или масла для купания «Липобейз baby», на протяжении 30 дней участия в протоколе.
Обсуждение
Потребность в регулярном, долгосрочном использовании средств лечебной косметики пациентами с атопическим дерматитом как один из ключевых компонентов достижения контроля и удержания ремиссии в настоящее время не вызывает сомнения у практикующих дерматологов и аллергологов [13, 14]. В то же время для пациентов и их родителей особенно важно мнение постоянно наблюдающего педиатра широкого профиля, а не только врачей-консультантов. Вот почему для сохранения приемлемого уровня комплайенса необходимо знакомить широкую педиатрическую аудиторию с новыми исследованиями по оценке эффективности использования лечебной косметики у детей с атопическим дерматитом. Настоящую работу отличает применение доступной гаммы средств отечественного производства в целях лечебного ухода за атопичной кожей, что может быть дополнительным мотивирующим фактором для отдельных пациентов при выборе лечебного комплекса [10, 15]. Для пациентов с легким/среднетяжелым течением атопического дерматита в дошкольном возрасте расход увлажняющего крема в количестве 1 упаковки за 2 нед может быть признан минимально достаточным; у некоторых более крупных детей или при более выраженных проявлениях можно рекомендовать и более интенсивное использование, до 1 упаковки в неделю [7, 15].
Представляется интересным, что независимо от ключевого триггера обострений даже у пациентов без пищевой сенсибилизации была показана эффективность комплекса увлажняющих препаратов «Липо-бейз baby» (крем и масло для купания). Понимание наличия разных фенотипов и клинико-патогенетических вариантов атопического дерматита активно обсуждается в актуальной медицинской периодике, однако подчеркивается, что базовый уход за кожей необходим всем пациентам, независимо от ведущего патогенетического звена атопического дерматита [16, 17].
В представленной работе показано повышение эффективности терапии атопического дерматита при использовании комплекса средств увлажнения кожи. Важно, что у отдельных пациентов применение этого комплекса начато в фазу обострения заболевания. Вопрос о сроках назначения лечебной косметики и возможности ее сочетания с фармакологическими противовоспалительными лекарственными препаратами нередко встает перед практикующими врачами. Дополнительное подтверждение безопасности и эффективности раннего назначения увлажняющих средств отвечает требованиям современных клинических рекомендаций [7, 8] и будет способствовать внедрению такого подхода в широкую клиническую практику.
Наши данные по положительной динамике ключевого объективного показателя контроля за течением атопического дерматита — индекса SCORAD — сопоставимы с результатами других работ [10, 14, 15] и подтверждают возможность рекомендации линейки «Липобейз baby крем» и «Липобейз baby масло» для купания для эффективного ведения детей с атопическим дерматитом как на этапе обострения, так и ремиссии основного заболевания. Показатели зуда и нарушения сна выбраны как в наибольшей степени ухудшающие качество жизни компоненты патогенеза атопического дерматита у пациентов первых 3 лет жизни. Кроме того, показано, что неукротимый зуд, особенно, ведущий к нарушению сна, существенно влияет на психомоторное развитие детей [9, 11].
Купирование и долгосрочный контроль этого показателя меняют течение атопического дерматита и восприятие этого заболевания пациентом и родителями.
Гамма «Липобейз baby» эффективна для контроля обоих субъективных показателей течения дерматита.
В целом средства лечебной косметики «Липобейз baby крем» и масло для купания показали высокую эффективность в достижении и удержании ремиссии у детей раннего возраста (0,5—3 лет жизни) с атопическим дерматитом легкого и среднетяжелого течения при начале терапии как в фазу обострения, так и ремиссии заболевания. Показана высокая удовлетворенность наблюдающих врачей и родителей пациентов проводимым лечением. Не зарегистрировано случаев нежелательных явлений либо непереносимости, связанных с использованием гаммы «Липобейз baby». Полученные в настоящем протоколе результаты в отношении скорости достижения ремиссии у больных атопическим дерматитом, динамики индекса SCORAD и показатели удовлетворенности пациентов и наблюдающих врачей сопоставимы с результатами апробаций немецких и французских косметических средств, ранее проводившихся авторами [18, 19].
ЛИТЕРАТУРА (REFERENCES)
1. Смирнова Г.И. Актуальный атопический дерматит: проблемы и перспективы. Российский аллергологический журнал 2017; 14: 4—5: 30—39. [Smirnova G.I. Actual atopic dermatitis: problemsand perspectives. Rossiiskii allergo-logicheskii zhurnal 2017; 14: 4-5: 30-39. (in Russ)]
2. Mortz C.G., Andersen K.E., Dellgren C., Barington T., Bindslev-Jensen C. Atopic dermatitis from adolescence to adulthood in the TOACS cohort: prevalence, persistence and comorbidities. Allergy 2015; 70(7): 836-845. DOI: 10.1111/all.12619
3. Al-naqeeb J., Danner S., Fagnan L.J., Ramsey K., Michaels L.A., Mitchell J. et al. The Burden of Childhood Atopic Dermatitis in the Primary Care Setting: A Report from the Meta-LARC Consortium. J Am Board Fam Med 2019; 32(2): 191-200. DOI: 10.3122/jabfm.2019.02.180225
4. Mallol J., Crane J., von Mutius E., Odhiambo J., Keil U., Stewart A.; ISAAC Phase Three Study Group. The International Study of Asthma and Allergies in Childhood (ISAAC) Phase Three: a global synthesis. Allergol Immunopathol ( Madr) 2013; 41(2): 73-85. DOI: 10.1016/j.aller.2012.03.001
5. Батожаргалова Б.Ц., Мизерницкий Ю.Л., Подольная М.А. Метаанализ распространенности астмоподобных симптомов и бронхиальной астмы в России (по результатам программы ISAAC). Российский вестник перинатологии и педиатрии 2016; 61(4): 59-69. [Batozhargalova B.C., Mizernickij Yu.L., Podol’naja M.A. Metanalysis of the prevalence of asthma-like symptoms and bronchial asthma in Russia (ISAAC program results). Rossiyskiy Vestnik Perinatologii i Pediatrii ( Russian Bulletin of Perinatology and Pediatrics) 2016; 61(4): 59-69. (in Russ)]. DOI: 10.21508/1027-40652016-61-4-59-69
6. Simpson E.L., Chalmers J.R., Hanifin J.M., Thomas K.S., Cork M.J., McLean W.H. et al. Emollient enhancement of the skin barrier from birth offers effective atopic dermatitis prevention. J Allergy Clin Immunol 2014; 134: 818-823. DOI: 10.1016/j.jaci.2014.08.005
7. Атопический дерматит у детей. Федеральные клинические рекомендации. М., 2016; 60. [Atopic dermatitis in children. Federal clinical recommendations. Moscow, 2016; 60. (in Russ)]
8. Werfel T., Heratizadeh A., Aberer W., Ahrens F., Augustin M., Biedermann T. et al. S2k guideline on diagnosis and treatment of atopic dermatitis - short version. Allergo J Int 2016; 25: 82-95. DOI: 10.1007/s40629-016-0110-8
9. Скрипкин Ю. К., Зверькова Ф.А., Шарапова Г.Я., Студ-ницын А.А. Руководство по детской дерматовенерологии. Ленинград: Медицина, 1983; 477. [Skripkin Yu. K., Zver’kova F.A., Sharapova G.Ja., Studnicyn A.A. Pediatric dermatovenerology guideline. Lenigrad: Meditsina, 1983; 477. (in Russ)]
10. Зайцева С.В., Застрожина А.К., Муртазаева О.А. Наружная терапия атопического дерматита у детей. Медицинский совет 2017; 19: 149-152. [Zajceva S.V., Zastrozhi-na A.K., Murtazaeva O.A. Topical therapy of atopic dermatitis in children. Medicinskii sovet 2017; 19: 149-152. (in Russ)]
11. Смирнова Г.И. Атопический дерматит у детей: новое в патогенезе, диагностике и лечении. Лечащий врач 2017; 4: 12-18. [Smirnova G.I. Atopic dermatitis in children: news in pathogenesis, diagnostics and treatment. Lechashchii vrach 2017; 4: 12-18. (in Russ)]
12. Severity scoring of atopic dermatitis: the SCORAD index. Consensus Report of the European Task Force on Atopic Dermatitis. Dermatol 1993; 186(1): 23-31.
13. Weidinger S., Novak N. Atopic dermatitis. Lancet 2016; 387:1109.
14. Балаболкин И.И., Булгакова В.А., Елисеева Т.И. Нарушение кожного барьера и продукты лечебной косметики для ухода за кожей при атопическом дерматите у детей. Фарматека 2018; S1: 64-71. [Balabolkin I.I., Bulgakova V.A., Eliseeva T.I. Skin barrier impairment and medical cosmetic skin care products for atopic dermatitis in children. Pharmateca 2018; S1: 64-71. (in Russ)]
15. Камаев А.В., Трусова О.В., Ляшенко Н.Л., Макарова И.В. Эмоленты в терапии атопического дерматита у детей: анализ клинической и фармакоэкономической эффективности. Российский аллергологический журнал 2017; 14(4-5): 98-107. [Kamaev A.V., Trusova O.V., Lja-shenko N.L., Makarova I.V. Emolients in atopic dermatitis treatment in children: analysis of clinical and pharmacoeconomical efficacy. Rossiiskii allergologicheskii zhurnal 2017; 14(4-5): 98—107. (in Russ)]
16. Cabanillas B., Brehler A.C., Novak N. Atopic dermatitis phenotypes and the needfor personalized medicine. Curr Opin Allergy Clin Immunol 2017; 17: 309-315. DOI: 10.1097/ ACI.0000000000000376
17. Roduit C., Frei R., Depner M., Karvonen A.M., Renz H., Braun-Fahrlander C. et al. Phenotypes of Atopic Dermatitis Depending on the Timing of Onset and Progression in Childhood. JAMA Pediatr 2017; 171(7): 655-662. DOI: 10.1001/ jamapediatrics.2017.0556
18. Макарова И.В. Уход за кожей больных атопическим дерматитом. Аллергология 2005; 1: 47-52. [Makarova I.V. Skin care for atopic dermatitis patients. Allergologiya 2005; 1: 47-52. (in Russ)]
19. Макарова И.В. Комплексный подход к наружной терапии детей с атопическим дерматитом с использованием средств ухода за кожей серии Бальнеум. Вопросы практической педиатрии 2007; 2(6): 60-64. [Makarova I.V. Complex approach to the topic therapy in children with atopic dermatitis: Balneum skin care products usage. Voprosy prakticheskoi pediatrii 2007; 2(6): 60-64. (in Russ)]
Поступила: 03.04.19
Конфликт интересов:
Препараты лечебной косметики для использования в настоящем протоколе предоставлены производителем ООО «Фармтек». В статистической обработке, интерпретации результатов и подготовке настоящей публикации представители компании-производителя участия не принимали.
Авторы данной статьи подтвердили отсутствие конфликта интересов и финансовой поддержки, о которых необходимо сообщить.